บททบทวนวารสาร
Review Article
สายระบายทรวงอกชนิดฝังใต้ผิวหนัง
(Tunneled pleural catheters)
สรายุทธ เอี่ยมสอาด พ.บ.*
ศุภฤกษ์ ดิษยบุตร พ.บ.
แจ่มศักดิ์ ไชยคุนา พ.บ.
*แพทย์เฟลโลว์ อนุสาขาหัตถการวินิจฉัยและรักษาโรคระบบการหายใจ
สาขาวิชาโรคระบบการหายใจและวัณโรค ภาควิชาอายุรศาสตร์
คณะแพทยศาสตร์ศิริราชพยาบาล มหาวิทยาลัยมหิดล
บทนำ
Tunneled pleural catheter (TPC) หรือ indwelling pleural catheter (IPC) คือ สายระบายทรวงอกชนิดหนึ่งซึ่งสามารถใส่คาไว้ได้เป็นเวลานาน ประโยชน์ที่สำคัญของการใส่สาย TPC นี้ คือช่วยบรรเทาอาการเหนื่อยของผู้ป่วยที่มีน้ำในช่องเยื่อหุ้มปอดและสามารถใส่แบบผู้ป่วยนอกได้โดยไม่จำเป็นต้องพักรักษาตัวในโรงพยาบาล และทำให้มีคุณภาพชีวิตดีขึ้น ปัจจุบันมีคำแนะนำในการใส่สาย TPC ในผู้ป่วยที่มีน้ำในช่องเยื่อหุ้มปอดทั้งที่มีสาเหตุจากมะเร็งแพร่กระจายและไม่ใช่มะเร็งซึ่งไม่ตอบสนองต่อการรักษาจำเพาะ นอกจากนี้ยังมีรายงานการใช้ในผู้ป่วยที่มีน้ำในช่องท้องปริมาณมากด้วย
ส่วนประกอบของสายระบาย TPC
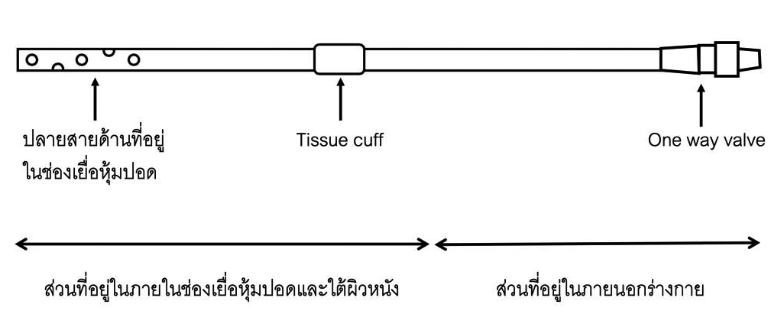
- สายระบายทรวงอก ทำมาจาก soft silicone ซึ่งเป็นวัสดุที่มีความเหนียวและยืดหยุ่นสูง มีหลายขนาดและความยาวแตกต่างกันขึ้นกับผลิตภัณฑ์ สายระบายประกอบด้วยส่วนต่าง ๆ ดังนี้ (รูปที่ 1)
- ปลายสายด้านหนึ่งที่อยู่ในช่องเยื่อหุ้มปอด จะมีรูด้านข้างเพื่อระบายน้ำในช่องเยื่อหุ้มปอด
- ส่วนกลางสายจะถูกฝังในชั้นใต้ผิวหนังซึ่งมี tissue cuff เพื่อชักนำให้เกิดการยึดเกาะกับเนื้อเยื่อใต้ผิวหนังได้ป้องการเลื่อนหลุดของสาย
- ปลายสายที่อยู่นอกช่องเยื่อหุ้มปอด จะมีส่วนต่อไปยังขวดเก็บน้ำในช่องเยื่อหุ้มปอด ซึ่งจะมีลิ้นควบคุมการไหลแบบทางเดียว (one way valve) หรือ clamp เพื่อป้องกันการไหลย้อนกลับทางของน้ำเข้าไปในช่องเยื่อหุ้มปอด
- ขวดระบายหรือถุงเก็บน้ำในช่องเยื่อหุ้มปอด มีหลายชนิด เช่น ขวดแรงดันลบ (vacuum bag) และขวดที่มีกระเปาะกดแบบ manual pump
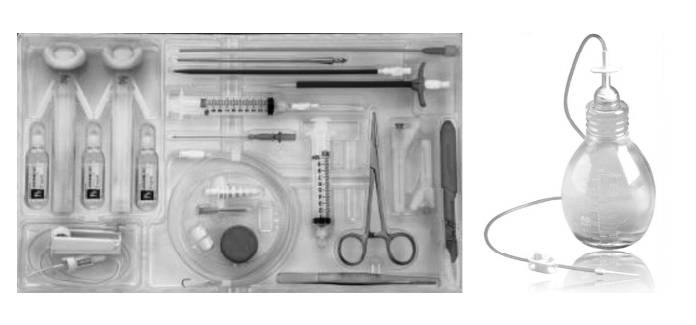
สายระบาย TPC ที่มีจำหน่ายในปัจจุบัน(1)
- PleuRx® catheter (Denver Biomedical, Golden Colorado) ดังแสดงในรูปที่ 2
- Aspira® pleural drain system (Bard Access Systems, Salt Lake City, Utah) มีออกแบบที่คล้ายคลึงกับ PleuRx® ต่างกันตรงที่ PleuRx® ใช้ขวดระบายแบบแรงดันลบ แต่ Aspira® ทำกระเปาะสำหรับดูดระบายน้ำโดยการทำ manual pump
- Rocket® Medical (Washington, Tyne & Wear, UK) มีออกแบบที่คล้ายคลึงกับ PleuRx® เพียงแต่มีลักษณะของสาย TPC และรูปลักษณ์ของขวดระบายแบบแรงดันลบที่ต่างไปเล็กน้อย ดังแสดงในรูปที่ 3
- The Relief® system (Med-italia Biomedica, Genoa, Italy) ลักษณะคล้ายคลึง PleuRx®
- สายระบายชนิดอื่นๆ ที่มีรายงานการนำมาใช้ ได้แก่ Tenckhoff catheter สำหรับใช้ล้างไตทางผนังช่องท้องมีรายงานนำมาใช้เป็นสารระบายทรวงอกในปี 19862, Port-A-Cath สำหรับการให้ยาเคมีบำบัดทางหลอดเลือดดำและสาย silicone ที่แบบไม่มี tissue cuff โดยต่อเข้ากับขวดระบาย Jackson drain (รูปที่ 4) ก็มีรายงานการนำมาใช้ในปี 2011 3


ข้อบ่งชี้ในการใส่สายระบาย TPC เพื่อระบายน้ำในช่องเยื่อหุ้มปอด
- น้ำในช่องเยื่อหุ้มปอดจากมะเร็งแพร่กระจาย (malignant pleural effusion, MPE)
- ภาวะปอดไม่ขยายตัว (trapped lung)
- ภาวะที่มีการสะสมของน้ำในช่องเยื่อหุ้มปอดจากสาเหตุอื่นที่ไม่ใช่มะเร็ง (recurrent non-malignant pleural effusion) เช่น ภาวะหัวใจวายเรื้อรัง (chronic congestive heart failure) และ hepatic hydrothorax ที่ได้รับการรักษาแบบมาตรฐานของโรคนั้น ๆ แล้วยังไม่ดีขึ้น
การใส่สายระบาย TPC ในผู้ป่วยที่มีน้ำในช่องเยื่อหุ้มปอดจากมะเร็งแพร่กระจาย
วัตถุประสงค์หลักในการรักษา MPE คือ รักษาอาการหอบเหนื่อย ประกอบด้วยหลายวิธี 4 ได้แก่
- การรักษาจำเพาะ ได้แก่ การให้ยาเคมีบำบัด
- การเฝ้าสังเกตอาการ (observation) กรณีไม่มีอาการ
- การผนึกเยื่อหุ้มปอด (pleurodesis) โดยการใส่ยาผนึกเยื่อหุ้มปอดผ่านทางสายระบายทรวงอกหรือการส่องกล้องช่องเยื่อหุ้มปอด (pleuroscopy) หรือการผ่าตัด โดยปัจจุบันมีคำแนะนำให้ประเมินก่อนว่าผู้ป่วยจะได้ประโยชน์จากการใส่สายระบายร่วมกับการผนึกเยื่อหุ้มปอดหรือไม่ เช่น ไม่มีสาเหตุอื่นที่ทำให้เกิดอาการหอบเหนื่อย อาการดีขึ้นหลังการเจาะระบายและมีการสะสมของน้ำกลับมาอย่างรวดเร็วจนก่อให้เกิดอาการ มีอัตราการรอดชีวิตไม่สั้นเกินไป เป็นต้น 5
- การใส่สายระบายทรวงอกชนิดฝังใต้ผิวหนัง (tunneled pleural catheter, TPC)
ในช่วงทศวรรษที่ผ่านมา มีการใส่สายระบาย TPC ในผู้ป่วยที่มีน้ำในช่องเยื่อหุ้มปอดจากมะเร็งแพร่กระจายมากขึ้น เนื่องจากทำได้ไม่ยากและสามารถให้การรักษาเป็นแบบผู้ป่วยนอกได้ ทำให้ผู้ป่วยมีอาการเหนื่อยดีขึ้นร้อยละ 96 และสามารถเกิด spontaneous pleurodesis ได้ถึงร้อยละ 656-7 การระบายน้ำแบบทุกวัน (aggressive drainage) อาจมีผลทำให้เกิด spontaneous pleurodesis ได้มากขึ้นเนื่องจาก parietal pleural มีโอกาสชิดกับ visceral pleural มากขึ้น มีการศึกษาเปรียบเทียบการเกิด spontaneous pleurodesis ในผู้ป่วยที่ได้รับการระบายน้ำทุกวันกับระบายน้ำแบบวันเว้นวัน พบว่าเกิด spontaneous pleurodesis ร้อยละ 47 และ 24 ในกลุ่มที่ระบายน้ำทุกวันและวันเว้นวันตามลำดับ โดยมีระยะเวลาการเกิดเท่ากับ 54 และ 90 วันตามลำดับ แต่ภาวะแทรกซ้อน คุณภาพชีวิตและความพึงพอใจของผู้ป่วยทั้งสองกลุ่มไม่แตกต่างกันอย่างมีนัยสำคัญทางสถิติ 8
มีการศึกษาการใส่สายระบาย TPC ในผู้ป่วย MPE เทียบกับการรักษาโดยวิธีอื่น เช่น การผนึกเยื่อหุ้มปอดโดย talc slurry หรือ poudrage หรือ surgical pleurodesis พบว่าการลดอาการหอบเหนื่อยและอัตราการรอดชีวิตไม่แตกต่างกัน แต่กลุ่มที่ใส่สายระบาย TPC ไม่จำเป็นต้องนอนโรงพยาบาลหรือมีระยะเวลาการนอนโรงพยาบาลสั้นกว่า 9-10
มีรายงานการใส่สายระบาย TPC ร่วมกับการผนึกเยื่อหุ้มปอดโดยผ่านทาง medical thoracoscopy ซึ่งเรียกว่า rapid pleurodesis พบว่ากลุ่มที่ใส่สายระบายมีระยะเวลาการนอนโรงพยาบาลเฉลี่ย 2 วัน สามารถถอดสาย TPC ออกได้ใน 8 วัน และมี pleurodesis success rate ถึงร้อยละ 94 โดยไม่พบภาวะแทรกซ้อนรุนแรง 11 และมีการศึกษาการทำ talc slurry ผ่านทาง TPC พบว่ากลุ่มที่ทำ talc slurry มี pleurodesis success rate ที่วันที่ 35สูงกว่าการใส่สาย TPC เพียงอย่างเดียวอย่างมีนัยสำคัญทางสถิติ (ร้อยละ 43 และ 23 ตามลำดับ) 12
ปัจจุบันมีคำแนะนำให้พิจารณาการรักษาผู้ป่วยที่มีน้ำในช่องเยื่อหุ้มปอดจากมะเร็งแพร่กระจายโดยการใส่สาย TPC ดังแสดงในรูปที่ 5 5
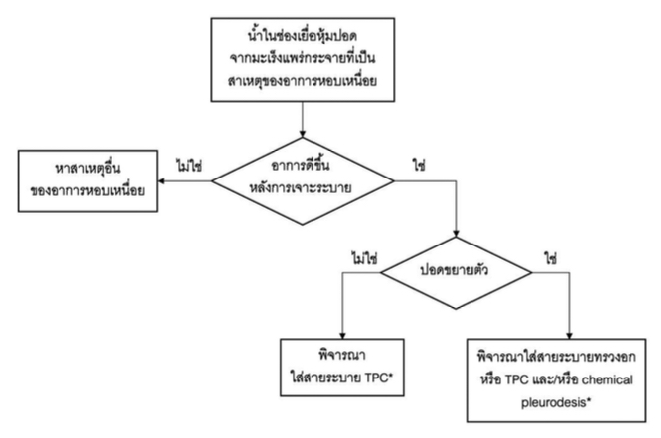
* ขึ้นกับดุลยพินิจของแพทย์ เช่น กรณีผู้ป่วยอาจมี short survival (เช่น อาจมีอัตราการรอดชีวิตไม่เกิน 1 สัปดาห์หรือ 1 เดือน) ไม่แนะนำให้ใส่สายระบายทรวงอก หรือสาย TPC
การใส่สายระบาย TPC ในผู้ป่วยที่มีน้ำในช่องเยื่อหุ้มปอดจากสาเหตุอื่นที่ไม่ใช่มะเร็ง
มีการศึกษามากขึ้นเกี่ยวกับการใส่สายระบาย TPC ในผู้ป่วยที่มีน้ำในช่องเยื่อหุ้มปอดจากสาเหตุอื่นที่ไม่ใช่มะเร็งที่ให้การรักษาจำเพาะอย่างเต็มที่แล้วยังไม่ดีขึ้นและมีอาการหอบเหนื่อยจากการมีน้ำในช่องเยื่อหุ้มปอด โดยโรคหรือภาวะที่มีข้อมูลมากที่สุดได้แก่ ภาวะหัวใจวายเรื้อรังและ hepatic hydrothorax ส่วนโรคหรือภาวะอื่น ๆ ที่มีรายงานเป็นกรณีศึกษา เช่น end stage renal disease with refractory pleural effusion, parapneumonic effusion/empyema, chylothorax, hydropneumothorax และ hemothorax เป็นต้น1,13-14 ข้อมูลจาก systematic review ของการใส่สาย TPC ในผู้ป่วย recurrent non-malignant pleural effusion จำนวน 325 ราย สาเหตุส่วนใหญ่ของน้ำในช่องเยื่อหุ้มปอด คือ chronic heart failure (ร้อยละ 49.8) มีอัตราการเกิด spontaneous pleurodesis ร้อยละ 42 และมีอัตราการเกิด empyema thoracis ร้อยละ 2.3 13
- Chronic heart failure ปัจจุบันมีการศึกษาแบบสุ่ม (TREAT-CHF) ในผู้ป่วย chronic heart failure ที่มี recurrent, chronic symptomatic pleural effusion โดยเปรียบเทียบผลของการรักษาโดยการใส่สาย TPC กับ การรักษาแบบมาตรฐาน คาดว่าจะเสร็จสิ้นประมาณปี พ.ศ. 2564
- Hepatic hydrothorax มีรายงานการศึกษาการใส่สาย TPC ในผู้ป่วย hepatic hydrothorax จำนวน 78 ราย โดยใส่เพื่อบรรเทาอาการร้อยละ 73 และใส่เพื่อบรรเทาอาการก่อนการผ่าตัด (bridging to surgery) ร้อยละ 27 พบว่าเกิด spontaneous pleurodesis ร้อยละ 22 โดยมีระยะเวลาเฉลี่ยตั้งแต่ใส่สายจนเกิด pleurodesis เท่ากับ 55 วัน โดยมีอัตราการเกิด pleural infection ร้อยละ 10 และร้อยละ 2.5 เสียชีวิตจาก catheter-related sepsis15
- Chylothorax การศึกษาของ Jimenez และคณะพบว่าเมื่อเปรียบเทียบระหว่างการใส่สายTPC และการรักษาประคับประคอง พบว่าการใส่สาย TPC ลดความเสี่ยงที่ต้องทำ second pleural intervention ได้อย่างมีนัยสำคัญทางสถิติ แม้ว่าจะมี serum albumin ลดต่ำลงในกลุ่มที่ใส่สาย TPC อย่างมีนัยสำคัญทางสถิติ แต่ระดับ serum albumin กลับมาเป็นปกติอย่างรวดเร็วหลังจากที่ถอดสายออก 14
- End stage renal disease (ESRD) มีอุบัติการณ์ของน้ำในช่องเยื่อหุ้มปอดประมาณร้อยละ 20 โดยสาเหตุส่วนใหญ่ คือ ภาวะน้ำเกิน (hypervolemia) รองลงเป็น congestive heart failure และ uremic pleuritis มีรายงานผู้ป่วย ESRD with refractory pleural effusion จำนวน 8 รายที่ได้รับการใส่สาย TPC โดยทุกรายมีอาการหอบเหนื่อยลดลง เกิด spontaneous pleurodesis ร้อยละ 37.5 และมีระยะเวลาเฉลี่ยในการเกิด spontaneous pleurodesis 46 วัน โดยไม่พบภาวะแทรกซ้อนรุนแรง 16
ข้อห้ามในการใส่สายระบาย TPC
- ผู้ป่วย ญาติ และบุคลากรทางการแพทย์ไม่สามารถให้การดูแลสายระบาย TPC ได้
- ภาวะแข็งตัวของเลือดผิดปกติที่ยังไม่ได้รับการแก้ไข หรือไม่สามารถแก้ไขได้
- ตำแหน่งที่จะใส่สายไม่เหมาะสม เช่น มีการติดเชื้อที่ผิวหนังและมีรอยโรคมะเร็งแพร่กระจายมาที่ผิวหนัง
- Multiloculated effusions และ ไม่มีช่องว่างในช่องเยื่อหุ้มปอด หรือมีพังผืดปริมาณมาก
ขั้นตอนการใส่สายระบาย TPC
ขั้นตอนอาจมีความแตกต่างกันไปในแต่ละผลิตภัณฑ์ แต่มีหลักการคล้ายกัน ดังนี้
- ทบทวนข้อบ่งชี้ในการใส่และข้อห้ามในการใส่สาย TPC
- ให้ข้อมูลแก่ผู้ป่วยและญาติ เกี่ยวกับข้อบ่งชี้ ขั้นตอนการทำหัตถการ ภาวะแทรกซ้อน และการดูแลผู้ป่วยและสายระบายหลังการทำหัตถการ และลงนามในใบยินยอมการทำหัตการ
- จัดท่าผู้ป่วยให้อยู่ในท่าที่เหมาะสม ได้แก่ ท่านอน และระบุตำแหน่งที่จะใส่สายระบาย (entry site) โดยยืนยันตำแหน่งด้วยอัลตราซาวด์
- ทายาฆ่าเชื้อที่ผิวหนัง ปูผ้าปราศจากเชื้อ
- ฉีดยาชาเฉพาะที่บริเวณ entry site และบริเวณที่จะให้สาย TPC จะโผล่ออกมานอกผิวหนัง (exit site) โดย exit site ควรอยู่ห่างจาก entry site ประมาณ 5 เซนติเมตร โดย entry site ควรอยู่บริเวณขอบบนของกระดูกซี่โครงล่างเพื่อป้องกันการบาดเจ็บต่อintercostal vessels
- ใช้ guide needle ต่อกับ syringe เจาะผ่านผิวหนังเข้าไปยังตำแหน่ง entry site เมื่อดูดได้น้ำในช่องเยื่อหุ้มปอดแล้วให้ใส่ guide wire เข้าไปในช่องเยื่อหุ้มปอด และเอา guide needle ออก
- ใช้มีดเปิดผิวหนังบริเวณ entry site และ exit site โดยไม่ควรให้แผลกว้างเกิน 1เซนติเมตรเนื่องจากอาจทำให้สายเลื่อนหลุดได้ง่าย
- นำ trocar ต่อเข้ากับปลายสาย TPC ด้านที่จะอยู่ในช่องเยื่อหุ้มปอดและแทง trocar ผ่านชั้นใต้ผิวหนัง (subcutaneous tissue) จาก exit site ไปยัง entry site โดยให้ tissue cuff อยู่ใต้ชั้นผิวหนังห่างจาก exit site ประมาณ 1 เซนติเมตร (หากใส่ลึกเกินไปอาจทำให้ดึงสายออกยากในกรณีที่ต้องการเอาสายออกภายหลัง) การทำเป็นช่องใต้ชั้นผิวหนัง (tunnel) นี้จะช่วยลดโอกาสการติดเชื้อได้
- ใช้ peel-away introducer ที่มี dilator อยู่ภายในร้อยเข้าไปใน guide wire จนเข้าไปอยู่ในช่องเยื่อหุ้มปอด หลังจากนั้นดึง guide wire พร้อม dilator ออกมาให้เหลือแต่ sheath ของ peel-away introducer
- ใส่สาย TPC ลงไปในช่องเยื่อหุ้มปอดโดยผ่านทาง sheath ของ peel-away introducer ในขณะเดียวกันให้ค่อย ๆ ฉีก sheath ออกจนสามารถใส่สาย TPC เข้าไปจนหมด ในขั้นตอนนี้ควรใส่สายด้วยความรวดเร็วและระมัดระวัง เพราะน้ำในช่องเยื่อหุ้มปอดอาจไหลออกมาในปริมาณมากหรืออากาศภายนอกอาจเข้าไปในช่องเยื่อหุ้มปอดได้ จากนั้นจึงเอา sheath ออก
- เย็บแผล entry site ส่วนแผล exit site อาจไม่จำเป็นต้องเย็บ และทำการยึดสาย TPC ไว้ให้มั่นคงเพื่อป้องกันการเลื่อนหลุด
- เริ่มระบายน้ำในช่องเยื่อหุ้มปอด โดยในครั้งแรกอาจพิจารณาระบายน้ำออกประมาณ 500-1,000 มิลลิลิตร แต่หากผู้ป่วยเริ่มมีอาการไอ แน่นหน้าอก หรือหอบเหนื่อยมากขึ้นให้หยุดระบายน้ำทันที
- ถ่ายภาพรังสีทรวงอกเพื่อดูตำแหน่งสายและภาวะแทรกซ้อนหลังทำหัตถการ
การดูแลหลังใส่สายระบาย TPC
- ปิดแผลให้มิดชิด และระวังไม่ให้โดนน้ำ
- สังเกตลักษณะและอาการผิดปกติที่เกิดกับแผลและผิวหนังโดยรอบ หากมีอาการผิดปกติดังต่อไปนี้ให้รีบพบแพทย์
2.1 มีอาการเจ็บหรือปวดบริเวณแผล
2.2 ผิวหนังโดยรอบมีอาการบวม แดงและร้อน
2.3 มีหนองหรือสารคัดหลั่งผิดปกติออกจากแผล
2.4 มีน้ำรั่วซึมออกมาโดยรอบ - ดูแลสายระบายไม่ให้หักงอ
คำแนะนำในการระบายน้ำโดยการใช้ขวดแรงดันลบ
ยังไม่มีคำแนะนำชัดเจนเกี่ยวกับความถี่ในการระบายน้ำในช่องเยื่อหุ้มปอดหลังการใส่สาย TPC มีการศึกษารายงานว่าการระบายน้ำทุกวันมีโอกาสเกิด spontaneous pleurodesis ภายใน 12 สัปดาห์ได้มากกว่าการระบายแบบวันเว้นวัน (ร้อยละ 47 และ 24 ตามลำดับ) โดยไม่เพิ่มอัตราการเกิดภาวะแทรกซ้อน เช่น การติดเชื้อ แต่อย่างไรก็ตามในผู้ป่วยที่มี trapped lung แนะนำให้พิจารณาระบายน้ำตามอาการและทำอย่างระมัดระวัง เนื่องจากผู้ป่วยอาจมีอาการเจ็บหน้าอก ไอ หรือหอบเหนื่อยได้หากมีการระบายน้ำมากเกินไป8
การระบายน้ำโดยการใช้ขวดแรงดันลบสามารถทำได้โดยผู้ดูแลหรือผู้ป่วยเอง โดยแพทย์ต้องมีการฝึกให้ทำอย่างถูกต้องด้วยเทคนิคปราศจากเชื้อ โดยมีขั้นตอนดังนี้
- เตรียมโต๊ะสะอาดและอุปกรณ์ต่าง ๆ ให้พร้อม และล้างมือให้สะอาด
- แกะผ้าก๊อสที่ปิดแผลและสายระบายออกอย่างระมัดระวัง ระวังการดึงรั้งสาย หากสังเกตว่าผิวหนังรอบ ๆ สายแดง บวม เจ็บ หรือมีหนอง ให้รีบไปพบแพทย์
- ล้างมือให้สะอาด และเปิดชุดอุปกรณ์และขวดระบายวางลงบนโต๊ะ โดยให้ปลายสายของสายที่ต่อกับขวดระบายวางอยู่ในชุดอุปกรณ์ซึ่งสะอาดปราศจากเชื้อ และใส่ถุงมือปราศจากเชื้อ
- ปิด clamp ที่อยู่บนสายระบายที่ต่อกับขวดระบายให้สนิท
- ถอดจุกที่ปิด one way valve ของสายระบายที่อยู่ที่ตัวผู้ป่วยออก และทำความสะอาดปลายสายบริเวณ one way valve ด้วยแอลกอฮอล์
- เสียบปลายสายระบายจากขวดระบายเข้ากับ one way valve ให้แน่น (ได้ยินเสียง “คลิก”)
- เริ่มการระบายน้ำโดยทำตามคำแนะนำในคู่มือของการใช้ขวดระบายแรงดันลบซึ่งอาจแตกต่างกันไปตามผลิตภัณฑ์ แนะนำให้ระบายน้ำออกครั้งละไม่เกิน 1,000 มิลลิลิตร หรือจนเมื่อมีอาการแน่นหรือเจ็บหน้าอก ไอมาก หรือหอบเหนื่อย หากเริ่มเกิดอาการดังกล่าวอาจลองปิด clamp บางส่วนหรือทั้งหมดและสังเกตอาการ หากอาการไม่ดีขึ้นให้หยุดระบายและพบแพทย์
- หลังจากระบายน้ำเสร็จเรียบร้อย ให้ดึงสายที่ต่อกับขวดระบายออก ทำความสะอาดปลาย one way valve ด้วยแอลกอฮอล์ และปิดด้วยจุดอันใหม่ให้แน่น
- ทำความสะอาดแผลรอบสายระบายตามคำแนะนำของแพทย์และปิดแผลให้เรียบร้อย
ภาวะแทรกซ้อนจากใส่สายระบาย TPC17
ภาวะแทรกซ้อนสัมพันธ์กับหัตถการ (Procedure-related complications) ได้แก่
- ภาวะลมในช่องเยื่อหุ้มปอด (pneumothorax) โดยปกติจะพบลมในช่องเยื่อหุ้มปอดหลังทำหัตการอยู่แล้วซึ่งเกิดจากอากาศภายนอกเข้าไประหว่างการทำหัตถการ แต่มักมีปริมาณไม่มากและไม่เพิ่มขึ้น หากพบมีลมในช่องเยื่อหุ้มปอดปริมาณมากหรือเพิ่มขึ้นหลังติดตามภาพรังสีทรวงอกและผู้ป่วยมีอาการหอบเหนื่อยมากขึ้นอาจเกิดจากการฉีกขาดของปอดที่เกิดจากการใส่สาย
- ภาวะเลือดออก อาจเกิดการบาดเจ็บของเส้นเลือด intercostal vessels ดังนั้นจึงควรเลือกตำแหน่งของ entry site ให้เหมาะสม
- Subcutaneous emphysema เกิดขึ้นระหว่างใส่สายได้ มักเป็นไม่มาก และดีขึ้นเรื่อย ๆ และหายไปในเวลาไม่นาน
- อาการปวดแผล มักเป็นใน 2-3 วันแรก ส่วนใหญ่บรรเทาด้วย simple analgesia แต่หากมีอาการปวดรุนแรงมากต้องนึกถึง intercostal nerve injury กรณีที่การรักษาประคับประคองอย่างเต็มที่แล้วยังไม่ทุเลาอาจจำเป็นจะต้องพิจารณาเอาสาย TPC ออก 18
ภาวะแทรกซ้อนที่เกิดจากใส่สายระยะยาว (catheter related complications) ได้แก่
- การติดเชื้อสัมพันธ์กับการใส่สายระบาย (catheter-related pleural infection) เช่น การติดเชื้อที่ผิวหนังด้านนอก (cellulitis), การติดเชื้อในช่องทางใต้ผิวหนัง (tunnel infection) และการติดเชื้อในช่องเยื่อหุ้มปอด (empyema thoracis) จากการศึกษาในผู้ป่วยที่ใส่สาย TPC เป็นระยะเวลานาน พบการอุบัติการณ์ของการติดเชื้อร้อยละ 1-9.6 17,19 และมีอัตราการเสียชีวิตร้อยละ 0.29 7 เชื้อก่อโรคส่วนใหญ่เกิดจาก Staphyloccous aureus, Pseudomonas aeruginosa และ Enterobacteriaceae ปัจจัยที่อาจมีผลต่อการติดเชื้อ เช่น การทำการระบายน้ำโดยผู้ป่วยเองหรือผู้ดูแล,ความถี่ในการระบาย เช่น ระบายน้ำทุกวันหรือวันเว้นจะพบการติดเชื้อมากกว่าการระบายสัปดาห์ละ 2 ครั้ง เป็นต้น การติดเชื้อส่วนใหญ่สามารถหายได้จากการให้การรักษาด้วยต้านจุลชีพชนิดรับประทานโดยไม่ต้องถอดสายออก แต่กรณี empyema thoracis อาจพิจารณารับผู้ป่วยไว้ในโรงพยาบาลเพื่อสังเกตอาการและให้ยาต้านจุลชีพทางหลอดเลือดดำ ในบางกรณีอาจต้องใส่สายระบายทรวงอกเพิ่ม และโอกาสน้อยมากที่ต้องถอดสายระบาย TPC ออก 5
- มะเร็งแพร่กระจายยังตำแหน่งที่ใส่สาย (catheter tract seeding/metastases) มีอุบัติการณ์ร้อยละ 5 พบบ่อยใน mesothelioma 20 เมื่อสงสัยจำเป็นจะต้องตัดชิ้นเนื้อส่งตรวจทางพยาธิวิทยาเพื่อยืนยันการวินิจฉัย และให้การรักษาโดยการฉายรังสีตรงตำแหน่งที่พบ แม้ว่า mesothelioma จะพบ seeding tract ได้บ่อยแต่ปัจจุบันยังไม่มีคำแนะนำให้ฉายรังสีเพื่อการป้องกัน
- Multiloculation เกิดขึ้นเนื่องจากมีการสะสมของ fibrinous material ทำให้เกิด septation ส่งผลให้การระบายน้ำลดลง อาจเป็นสาเหตุทำให้อาการหอบเหนื่อยแย่ลง โดยมีอุบัติการณ์ร้อยละ 5-14 21 มีการศึกษาวิจัยเกี่ยวกับการใช้ intrapleural fibrinolytic ทางสาย TPC พบว่าสามารถลดอาการหอบเหนื่อยได้ร้อยละ 83 ช่วยการระบายน้ำดีขึ้นร้อยละ 93 แต่พบภาวะเลือดออกหลังการใส่ยาร้อยละ 3 22
- เจ็บหน้าอก มีอุบัติการณ์ร้อยละ 36 มักมีอาการเจ็บไม่มาก ส่วนใหญ่เกิดจากการเจ็บปวดบาดแผลซึ่งเกิดภายหลังการทำหัตถการในช่วงแรก สาเหตุอื่น ๆ ได้แก่ trapped lung ซึ่งอาการปวดมักจะสัมพันธ์กับการระบายน้ำออก แก้ไขโดยการระบายน้ำช้า ๆ และทีละน้อย หรือหยุดระบายทันทีที่เริ่มมีอาการเจ็บหน้าอกหรือไอ
- ภาวะภูมิคุ้มกันลดลงและทุพโภชนาการ อาจเกิดเนื่องจาก chronic pleural drainage ทำให้มีอาการสูญเสียเซลล์และโปรตีนบางชนิดออกไปโดยเฉพาะในผู้ป่วยที่เป็นchylothorax 14
- สายเลื่อนหลุด (catheter dislodgement) พบอุบัติการณ์ร้อยละ 0.9-18 23-24 มักเกิดในช่วงแรกโดยสัมพันธ์กับการวางตำแหน่งของ tissue cuff ไม่เหมาะสม และผู้ป่วยมี wound healing ไม่ดีโดยเฉพาะผู้ป่วยที่มีภาวะ cancer-associated cachexia และผู้ป่วยที่ได้รับยาเคมีบำบัด
- สายตัน พบอุบัติการณ์น้อยกว่าร้อยละ 5 โดยมักเป็นแบบ partial obstruction มากกว่า 7 สาเหตุเกิดจากการสะสมของ fibrinous exudate ภายในสายหรือรอบ ๆ สาย สามารถแก้ไขโดยการไล่สายด้วยน้ำเกลือโดยใช้เทคนิคปราศจากเชื้อ หากไม่ได้ผลอาจพิจารณาใส่ fibrinolytic agent
- การรั่วซึมด้านข้างสาย TPC (peri-catheter leakage) พบอุบัติการณ์ร้อยละ 13 มักหายได้เองและน้อยมากที่ต้องการผ่าตัดแก้ไข สันนิษฐานว่าเกิดจากแรงดันภายในช่องทรวงอกที่สูงเป็นเหตุให้เกิดการรั่วรอบ ๆ สาย 25
- สายขาดขณะถอดสายออก (catheter fracture during removal) อาจเกิดขึ้นได้จากการฉุดรั้งของพังผืดที่หุ้มสาย โดยสัมพันธ์กับระยะเวลาที่ใส่สาย TPC จากการศึกษาพบว่า ส่วนของสาย TPC ที่ค้างอยู่ในร่างกายมักไม่ก่อให้เกินภาวะแทรกซ้อนใดๆ ดังนั้นไม่มีความจำเป็นจะต้องผ่าตัดเพื่อเอาชิ้นส่วนสายออก 26
ข้อบ่งชี้ของการถอดสาย TPC ออก
- เกิด spontaneous pleurodesis โดยสังเกตจากน้ำที่ระบายได้มีปริมาณลดลงร่วมกับภาพถ่ายรังสีทรวงอกพบน้ำไม่เพิ่มขึ้น หากภาพถ่ายรังสีทรวงอกพบว่าน้ำมีปริมาณเพิ่มขึ้น แต่ระบายน้ำไม่ออกให้พิจารณาแก้ไขภาวะสายอุดตันก่อน
- มีอาการเจ็บปวดมาก ซึ่งอาจเกิดจากการบาดเจ็บต่อ intercostal nerve
- มีการติดเชื้อ (empyema) ที่รักษาโดยการให้ยาต้านจุลชีพแล้วไม่ดีขึ้น
- มีการอุดตันของสาย ที่แก้ไขไม่ได้โดยการไล่สายด้วยน้ำเกลือหรือการใส่ fibrinolytic agent
- เสียชีวิต
สรุป
การใส่สายระบายทรวงอกชนิดฝังใต้ผิวหนัง(TPC) มีประโยชน์ในการลดอาการหอบเหนื่อยและเพิ่มคุณภาพชีวิตในผู้ป่วยที่มีน้ำในช่องเยื่อหุ้มปอดทั้งที่มีสาเหตุจากมะเร็งและไม่ใช่มะเร็งซึ่งไม่ตอบสนองกับการรักษาจำเพาะ นอกจากนี้ผู้ป่วยและผู้ดูแลสามารถระบายน้ำได้ด้วยตนเองโดยที่ไม่จำเป็นต้องพักรักษาตัวในโรงพยาบาล อย่างไรก็ตามแพทย์ผู้ดูแลจำเป็นต้องมีการคัดเลือกผู้ป่วยที่เหมาะสม และให้ความรู้และติดตามการรักษาอย่างใกล้ชิด
เอกสารอ้างอิง
- Bhatnagar R, Reid ED, Corcoran JP, et al. Indwelling pleural catheters for non-malignant effusions: a multicentre review of practice. Thorax 2014; 69:959-61.
- Bertolaccini L, Viti A, Paiano S, Pomari C, Assante LR, Terzi A. Indwelling pleural catheters: a clinical option in Trapped lung. Thorac Surg Clin 2017; 27:47-55.
- Tscheikuna J, Thomrongpairoj P, Disayabutr S. The efficacy of Jackson drain in the application to be a tunnel pleural catheter (TPC) in the management of malignant pleural effusion. J Med Assoc Thai 2011; 94:679-85.
- Koegelenberg CFN, Shaw JA, Irusen EM, Lee YCG. Contemporary best practice in the management of malignant pleural effusion. Ther Adv Respir Dis 2018; 12:1753466618785098.
- Feller-Kopman DJ, Reddy CB, DeCamp MM, et al. Management of malignant pleural effusions. An official ATS/STS/STR clinical practice guideline. Am J Respir Crit Care Med 2018; 198:839-49.
- Van Meter ME, McKee KY, Kohlwes RJ. Efficacy and safety of tunneled pleural catheters in adults with malignant pleural effusions: a systematic review. J Gen Intern Med 2011; 26:70-6.
- Fysh ETH, Tremblay A, Feller-Kopman D, et al. Clinical outcomes of indwelling pleural catheter-related pleural infections: an international multicenter study. Chest 2013; 144:1597-602.
- Wahidi MM, Reddy C, Yarmus L, et al. Randomized trial of pleural fluid drainage frequency in patients with malignant pleural effusions. The ASAP trial. Am J Respir Crit Care Med 2017; 195:1050-7.
- Bibby AC, Dorn P, Psallidas I, et al. ERS/EACTS statement on the management of malignant pleural effusions. Eur Respir J 2018; 52:1800349 [https//doi.org/10.1183/13993003.00349-2018].
- Iyer NP, Reddy CB, Wahidi MM, et al. Indwelling pleural catheter versus pleurodesis for malignant pleural effusions. A systematic review and meta-analysis. Ann Am Thorac Soc 2019; 16:124-31.
- Reddy C, Ernst A, Lamb C, Feller-Kopman D. Rapid pleurodesis for malignant pleural effusions: a pilot study. Chest 2011; 139:1419-23.
- Bhatnagar R, Keenan EK, Morley AJ, et al. Outpatient talc administration by indwelling pleural catheter for malignant effusion. New Engl J Med 2018; 378:1313-22.
- Patil M, Dhillon SS, Attwood K, Saoud M, Alraiyes AH, Harris K. Management of benign pleural effusions using indwelling pleural catheters: a systematic review and meta-analysis. Chest 2017; 151:626-35.
- Jimenez CA, Mhatre AD, Martinez CH, Eapen GA, Onn A, Morice RC. Use of an indwelling pleural catheter for the management of recurrent chylothorax in patients with cancer. Chest 2007; 132:1584-90.
- Shojaee S, Rahman N, Haas K, et al. Indwelling tunneled pleural catheters for refractory hepatic hydrothorax in patients with cirrhosis: a multicenter study. Chest 2019; 155:546-53.
- Potechin R, Amjadi K, Srour N. Indwelling pleural catheters for pleural effusions associated with end-stage renal disease: a case series. Ther Adv Respir Dis 2015; 9:22-7.
- Chalhoub M, Saqib A, Castellano M. Indwelling pleural catheters: complications and management strategies. J Thorac Dis 2018; 10:4659-66.
- Wrightson JM, Fysh E, Maskell NA, Lee YC. Risk reduction in pleural procedures: sonography, simulation and supervision. Curr Opin Pulm Med 2010; 16:340-50.
- Lui MM, Thomas R, Lee YC. Complications of indwelling pleural catheter use and their management. BMJ Open Respir Res 2016; 3(1):e000123.
- Sartori S, Nielsen I, Trevisani L, Tassinari D, Abbasciano V. Subcutaneous seeding after ultrasound-guided placement of intrapleural catheter. An unusual complication of the intracavitary palliative treatment of pleural mesothelioma. Support Care Cancer 1999 ;7:362-4.
- Chee A, Tremblay A. The use of tunneled pleural catheters in the treatment of pleural effusions. Curr Opin Pulm Med 2011; 17:237-41.
- Thomas R, Budgeon CA, Kuok YJ, et al. Catheter tract metastasis associated with indwelling pleural catheters. Chest 2014; 146:557-62.
- Tremblay A, Michaud G. Single-center experience with 250 tunnelled pleural catheter insertions for malignant pleural effusion. Chest 2006; 129:362-8.
- Van den toorn LM, Schaap E, Surmont VF, Pouw EM, van der Rijt KC, van Klaveren RJ. Management of recurrent malignant pleural effusions with a chronic indwelling pleural catheter. Lung Cancer 2005; 50:123-7.
- Chalhoub M, Ali Z, Sasso L, Castellano M. Experience with indwelling pleural catheters in the treatment of recurrent pleural effusions. Ther Adv Respir Dis 2016; 10:566-72.
- Fysh ETH, Wrightson JM, Lee YCG, Rahman NM. Fractured indwelling pleural catheters. Chest 2012; 141:1090-4.
